
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Практическое применение электрической проводимости
|
|
|
|
1. Определение fэ сильных электролитов:

2. Определение константы и степени диссоциации слабых электролитов:
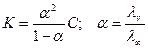
В не слишком разбавленных растворах величина a у слабых кислот и оснований очень мала, и можно считать, что 1 - a» 1. Тогда получаем:
K = a2 C и a = 
Это уравнение дает простой способ подсчета степени электролитической диссоциации слабого электролита в растворе данной концентрации, когда константа К известна.
 3. Определение солесодержания в растворе электролита:
3. Определение солесодержания в растворе электролита:
 1000 = Сi (lk + la)
1000 = Сi (lk + la)
Сi = 1000 / 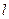 k +
k + 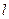 a
a
4. Определение растворимости труднорастворимых солей.
По закону действующих масс для бинарного электролита можно записать:
[K+] [A-] = K [KA] = ПР,
где ПР – произведение растворимости. ПР = const при Т = const
Если соединение диссоциирует нацело, то
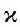 [K+] = [A-] = ÖПР = С (моль/л)
[K+] = [A-] = ÖПР = С (моль/л)
ПР и С определяют из данных насыщенного раствора электролита.
Пример: AgCl
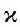
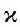 Сначала измеряют дистиллированной воды (=1,5×10-6См/м).
Сначала измеряют дистиллированной воды (=1,5×10-6См/м).
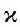 насыщенного раствора AgCl равна 2,75×10-6См/м.
насыщенного раствора AgCl равна 2,75×10-6См/м.
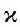 Следовательно:
Следовательно:
(AgCl) = 2,75×10-6 - 1,5×10-6 = 1,25×10-6 См/м
Электролитические подвижности ионов Ag+ и Cl- равны соответственно 53,8 и 65,2, а молярная электрическая проводимость при бесконечном разбавлении:
l¥ = 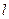 Ag +
Ag + 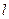 Cl = 53,5 + 65,2 = 119,0 См/м2
Cl = 53,5 + 65,2 = 119,0 См/м2
 Так как
Так как
l¥ = V;
то определяем V, содержащий 1 моль AgCl:

Число молей в 1 литре равно:
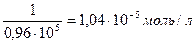
|
|
|
|
|
Дата добавления: 2014-12-27; Просмотров: 471; Нарушение авторских прав?; Мы поможем в написании вашей работы!