
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
ТЕРМОДИНАМИческие И ТЕРмохимические расчеты
Распределите валентные электроны по квантовым ячейкам в возбужденном состоянии атомов элементов, указанных в разделе 3.2.
Напишите значения четырех квантовых чисел для валентных электронов атомов элементов, указанных в разделе 3.2.
Определите электронное семейство элементов, указанных в разделе 3.2, распределите валентные электроны по квантовым ячейкам в не возбужденном состоянии атома. Поясните, металлические или неметаллические свойства имеет данный элемент с точки зрения строения атома.
3.5. Сравните свойства указанных элементов (радиусы атомов, их энергии ионизации, энергии сродства к электрону, электроотрицательности, а также химические свойства: металл – неметалл, восстановитель – окислитель) на основании строения атома:
| 01 – лития и фтора; | 02 – алюминия и галлия; |
| 03 – иттрия и индия; | 04 – марганца и брома; |
| 05 – натрия и хлора; | 06 – галлия и брома; |
| 07 – мышьяка и фосфора; | 08 – цезия и астата; |
| 09 – азота и висмута; | 10 – бериллия и радия; |
| 11 – кальция и цинка; | 12 – калия и брома; |
| 13 – молибдена и теллура; | 14 – селена и хрома; |
| 15 – фтора и астата; | 16 – лития и франция; |
| 17 – индия и йода; | 18 – кальция и железа; |
| 19 – углерода и олова; | 20 – ванадия и мышьяка; |
| 21 – углерода и свинца; 23 – меди и селена; | 22 – калия и меди; 24 – олова и технеция; |
| 25 – галлия и скандия; | 26 – азота и мышьяка; |
| 27 – фтора и хлора; | 28 – ртути и рения; |
| 29 – натрия и серы; | 30 – алюминия и хлора; |
3.7. Рассмотрите образование химических связей в молекулах с точки зрения метода валентных связей (МВС):
| 01 – PBr3 05 – CH3Br 09 – MgCl2 13 – PH3 17 – CH2Br2 21 – H2Se 25 – H2Te 29 – CCl4 | 02 – BF3 06 – CH2Cl2 10 – AlF3 14 – GaCl3 18 – ZnCl2 22 – CdCl2 26 – CO 30 – C2H2 | 03 – MgBr2 07 – AsCl3 11 – SiH4 15 – H2S 19 – GeH4 23 – SnCl4 27 – CHCl3 | 04 – SiF4 08 – NF3 12 – C2H4 16 – CHBr3 20 – AsH3 24 – SbH3 28 – SiО2 |
С этой целью определите:
- Валентные электроны взаимодействующих атомов, распределите их по квантовым ячейкам;
- механизм образования связей в молекуле,
- тип гибридизации центрального атома,
- геометрическую форму молекулы,
- число и тип связей (d или p - связи) в молекуле,
- полярность отдельных связей в молекуле ( полярны или неполярны),
- полярность молекулы в целом ( полярна или неполярна).
3.8. Составьте энергетические диаграммы и определите порядок связи в следующих частицах:
| 01 – CO+ 05 – C2 09 – F2 13 – I2 17 – Не2+ 21 – C2− 25 – O2+ 29 – NO+ | 02 – Be2 06 – BO 10 – B2 14 – CN 18 – N2− 22 – O2− 26 – H2+ 30 – H2− | 03 – CO 07 – Не2 11 – CN− 15 – Br2 19 – F2+ 23 – F2− 27 – NO− | 04 – N2 08 – NO 12 – BN 16 – O2 20 – B2− 24 – B2+ 28 – Cl2 |
Могут ли существовать указанные частицы? Ответ обоснуйте с точки зрения метода молекулярных орбиталей (ММО).
4.1. Составьте термохимические уравнения реакций и вычислите стандартную энтальпию образования D 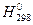 , (кДж/моль) следующих веществ:
, (кДж/моль) следующих веществ:
01 – MnBr2, если при образовании 5 г его выделилось 14,3 кДж;
02 – MnCl2, если при образовании 5 г его выделилось 19,3 кДж;
03 – MnS, если при образовании 5 г его выделилось 11,76 кДж;
04 – Na2O, если при образовании 10 г его выделилось 67,6 кДж;
05 – K2O, если при образовании 10 г его выделилось 38,6 кДж;
06 – Rb2O, если при образовании 10 г его выделилось 17,6 кДж;
07 – Cs2O, если при образовании 10 г его выделилось 9,24 кДж;
08 – CrCl3, если при образовании 17 г его выделилось 60,5 кДж;
09 – CdI2, если при образовании 20 г его выделилось 10,9 кДж;
10 – CdBr2, если при образовании 18 г его выделилось 21,0 кДж;
11 – CdF2, если при образовании 4,6 г его выделилось 21,2 кДж;
12 – CdCl2, если при образовании 9,6 г его выделилось 8,2 кДж;
13 – CaS, если при образовании 6 г его выделилось 40,3 кДж;
14 – CaCO3, если при образовании 10 г его выделилось 120,9 кДж;
15 – CBr4, если при образовании10 г его выделилось 3,78 кДж;
16 – BiCl3, если при образовании 2,4 г его выделилось 2,06 кДж;
17 – BeO, если при сгорании 15 г бериллия выделилось 1020,6 кДж;
18 – BaF2, если при образовании 3 г его выделилось 20,6 кДж;
19 – BaCl2, если при образовании 1,75 его выделилось 7,3 кДж;
20 – As2O5, если при сгорании 7 г мышьяка выделилось 40,8 кДж;
21 – Al2S3, если при образовании 3,5 г его выделилось 11,9 кДж;
22 – AlCl3, если при образовании 5 г его выделилось 26,2 кДж;
23 – AgF, если при образовании 3 г его выделилось 4,83 кДж;
24 – Ag2O, если при сгорании 4,5 г серебра выделилось 2,57 кДж;
25 – H2Se, если при образовании 2 л его (н.у.) поглотилось 7,68 кДж;
26 – PCl3, если при образовании 27,5 г его выделилось 55,9 кДж;
27 – SO2, если при сгорании 1 г серы выделилось 29,9 кДж;
28 – CO2, если при образовании 1 л CO2 (н.у.) выделилось 15,8 кДж;
29 – AlF3, если при образовании 2,1 г его выделилось 32,4 кДж;
30 – Cr2O3, если при образовании 3,8 г оксида выделилось 30,8 кДж.
4.2. Вычислите количество тепла (кДж), выделяющееся при образовании из простых веществ в стандартных условиях:
| 01 – 4,8 г оксида фосфора (III); 03 – 26,7 г хлорида алюминия; 05 – 16,9 г сульфида бария; 07 – 50,0 г оксида бериллия; 09 – 200 г оксида кальция; 11 – 17,4 г оксида марганца (IV); 13 – 47,8 г оксида свинца (IV); 15 – 18,0 г оксида кремния (IV); 17 – 79,8 г оксида теллура (IV); 19 – 24,0 г хлорида бериллия; 21 – 15,9 г оксида меди (II); 23 – 47,8 г сульфида меди (II); 25 – 3,04 г оксида хрома (III); 27 – 20 г оксида мышьяка (III); 29 – 0,5 г хлороводорода; | 02 – 26,7 г бромида алюминия; 04 – 45,0 г сульфида алюминия; 06 – 16,9 г оксида бария; 08 – 3,6 г сульфида кальция; 10 – 7,1 г оксида марганца (II); 12 – 44,6 г оксида свинца (II); 14 – 160 г оксида серы (VI); 16 – 105,5 г оксида олова (IV); 18 – 8,0 г оксида титана (IV); 20 – 10,7 г сульфида висмута (III); 22 – 47,8 г сульфида свинца (II); 24 – 0,27 г бромида алюминия; 26 – 3,6 г воды; 28 – 8,1 г селеноводорода; 30 – 1 г гидроксида натрия. |
4.3. Вычислите тепловой эффект процесса, D 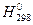 (кДж), протекающего в стандартных условиях, для следующих реакций:
(кДж), протекающего в стандартных условиях, для следующих реакций:
01 – 2Al(тв) + 3NiO(тв) = Al2O3(тв) + 3Ni(тв)
02 – BaCO3(тв) + C(тв) = BaO(тв) + 2CO2(г)
03 – 2BaO(тв) + O2(г) = 2BaO2(тв)
04 – 3BaO(тв) + 2Al(тв) = 3Ba(тв) + Al2O3(тв)
05 – CaO(тв) + H2O(ж) = Ca(OH)2(тв)
06 – CaO(тв) + CO2(г) = CaCO3(тв)
07 – 2MgO(тв) + Si(тв) = 2Mg(тв) + SiO2(тв)
08 – Cr2O3(тв) + 2Al(тв) = 2Cr(тв) + Al2O3(тв)
09 – 3CuO(тв) + 2Al(тв) = 3Cu(тв) + Al2O3(тв)
10 – 3CuO(тв) + 2Fe(тв) = 3Cu(тв) + Fe2O3(тв)
11 – 2CuO(тв) + C(тв) = 2Cu(тв) + CO2(г)
12 – 2 AgF(тв) + H2(г) = 2Ag(тв) + 2HF(г)
13 – Ag2O(тв) + CO(г) = 2Ag(тв) + CO2(г)
14 – Ag2O(тв) + H2(г) = 2Ag(тв) + H2O(ж)
15 – Na2O2(тв) + 2Na(тв) = 2Na2O(тв)
16 – 2NaOH(тв) + 2Na(тв) = 2Na2O(тв) + H2(г)
17 – 4 NaOH(тв) + 3Fe(тв) = 4Na(тв) + Fe3O4(тв) + 2H2(г)
18 – 2Na2CO3(тв) + 3Fe(тв) = 4Na(тв) + Fe3O4(тв) + 2CO(г)
19 – 2NaHCO3(тв) = Na2CO3(тв) + H2O(ж) + CO2(г)
20 – Na2CO3(тв) + 2C(тв) = 2Na(г) + 3CO(г)
21 – 2NaOH(тв) + C(тв) = 2Na(тв) + CO(г) + H2O(ж)
22 – 3Fe(тв) + 2O2(г) = Fe3O4(тв)
23 – 2FeO(тв) + Si(тв) = 2Fe(тв) + SiO2(тв)
24 – Fe2O3(тв) + 3CO(г) = 2Fe(тв) + 3CO2(г)
25 – FeO(тв) + CO(г) = Fe(тв) + CO2(г)
26 – Fe3O4(тв) + CO(г) = 3FeO(тв) + CO2(г)
27 – 3Fe2O3(тв) + CO(г) = 2Fe3O4(тв) + CO2(г)
28 – 3Fe3O4(тв) + 8Al(тв) = 9Fe(тв) + 4Al2O3(тв)
29 – Fe2O3(тв) + 2Al(тв) = 2Fe(тв) + Al2O3(тв)
30 – Fe2O3(тв) + 3H2(г) = 2Fe(тв) + 3H2O(ж).
4.4. Вычислите изменение стандартной энтропии, D 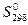 (Дж/К), при протекании следующих процессов:
(Дж/К), при протекании следующих процессов:
01 – CO2(г) + CaO(тв) = CaCO3(тв)
02 – CO2(г) + BaO(тв) = BaCO3(тв)
03 – B2O3(тв) + 3Mg(тв) = 2B(тв) + 3MgО(тв)
04 – KClO4(тв) = KCl(тв) + 2O2(г)
05 – SO2(г) + 0,5O2(г) = SO3(г)
06 – PbS(тв) + 4O3(г) = PbSO4(тв) + 4O2(г)
07 – CuS(тв) + 1,5O2(г) = CuO(тв) + SO2(г)
08 – 2CO(г) + O2(г) = 2CO2(г)
09 – 2Al(тв) + 3S(тв) = Al2S3(тв)
10 – Al(тв) + 1,5Cl2(г) = AlCl3(тв)
11 – Al(тв) + 1,5Br2(ж) = AlBr3(ж)
12 – Al(тв) + 1,5I2(тв) = AlI3(тв)
13 – 2Ag(тв) + Cl2(г) = 2AgCl(тв)
14 – BeO(тв) + Mg(тв) = MgO(тв) + Be(тв)
15 – CS2(ж) + 3O2(г) = CO2(г) + 2SO2(г)
16 – C(ГРАФИТ) + 2S(тв) = CS2(ж)
17 – Be(тв) + Cl2(г) = BeCl2(тв)
18 – CdS(тв) + 1,5O2(г) = CdO(тв) + SO2(г)
19 – 3FeO(тв) + 0,5O2(г) = Fe3O4(тв)
20 – 2FeO(тв) + 0,5O2(г) = Fe2O3(тв)
21 – H2(г) + S(тв) = H2S(г)
22 – H2S(г) + 1,5O2(г) = H2O(ж) + SO2(г)
23 – I2(тв) + Br2(ж) = 2IBr(г)
24 – I2(тв) + 3Cl2(г) = 2ICl3(тв)
25 – H2O2(ж) = H2O(ж) + 0,5O2(г)
26 – Fe2O3(тв) + 3H2(г) = 2Fe(тв) + 3H2O(ж)
27 – Fe3O4(тв) + 4CO(г) = 3Fe(тв) + 4CO2(г)
28 – 3Fe(тв) + 4H2O(ж) = Fe3O4(тв)+ 4H2(г)
29 – CuO(тв) + H2(г) = Cu(тв) + H2O(ж)
30 – Fe2O3(тв) + CO(г) = 2FeO(тв) + CO2(г).
4.5. Вычислите изменение стандартной энергии Гиббса, D 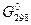 (кДж), и определите возможность осуществления в стандартных условиях следующих реакций:
(кДж), и определите возможность осуществления в стандартных условиях следующих реакций:
01 – AgF(тв) + 0,5Cl2(г) = AgCl(тв) + 0,5F2(г)
02 – Be(тв) + H2O(ж) = BeO(тв) + H2(г)
03 – B2O3(тв) + 3CO(г) = 2B(тв) + 3CO2(г)
04 – BaO2(тв) + CO(г) = BaCO3(тв)
05 – BaO2(тв) = BaO(тв) + 0,5O2(г)
06 – BaCO3(тв) = BaO(тв) + CO2(г)
07 – BaO(тв) + H2(г) = Ba(тв) + H2O(ж)
08 – BaO(тв) + C(ГРАФИТ) = Ba(тв) + CO(г)
09 – BaO(тв) + CO(г) = Ba(тв) + CO2(г)
10 – B2O3(тв) + 3H2(г) = 2B(тв) + 3H2O(ж)
11 – 2C(ГРАФИТ) + 4Al(тв) = Al4C3(тв)
12 – 2B(тв) + 3H2(г) = B2H6(г)
13 – 2HI(г) + 0,5O2(г) = H2O(ж) + I2(тв)
14 – 2HBr(г) + 0,5O2(г) = H2O(ж) + Br2(ж)
15 – 2H2(г) + Si(тв) = SiН4(г)
16 – P(тв) + 1,5H2(г) = PH3(г)
17 – CaCO3(тв) = CaO(тв) + CO2(г)
18 – 2HCl(г) + O3(г) = Cl2(г) + H2O(ж) + O2(г)
19 – 2HF(г) + 0,5O2(г) = H2O(ж) + F2(г)
20 – H2O(ж) + O3(г) = H2O2(ж) + O2(г)
21 – 0,5Cl2(г) + O2(г) = ClO2(г)
22 – CS2(ж) + 3O2(г) = CO2(г) + 2SO2(г)
23 – CO2(г) + 2H2S(г) = CS2(г) + 2H2O(ж)
24 – COS(г) + H2O(ж) = CO2(г) + H2S(г)
25 – CO2(г) + 2HCl(г) = COCl2(г) + H2O(ж)
26 – BaO(тв) + SO3(г) = BaSO4(тв)
27 – CH4(г) + 3CO2(г) = 4CO(г) + 2H2O(ж)
28 – Mg(тв) + CO2(г) = MgO(тв) + CO(г)
29 – MgCO3(тв) = MgO(тв) + CO2(г)
30 – CO(г) + S(г) = COS(г).
4.6. Вычислите изменение энергии Гиббса, DG0 (кДж), следующих реакций, протекающих при указанной температуре (зависимостью D 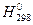 и D
и D 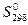 от температуры пренебречь):
от температуры пренебречь):
| Вариант | Уравнение реакции | Т, К |
| 1. | CaCO3(тв) = CaO(тв) + CO2(г) | |
| 2. | CH4(тв) + 3CO2(г) = 4CO(г) + 2H2O(г) | |
| 3. | Ag2O(тв) + H2(г) = 2Ag(тв) + H2О(г) | |
| 4. | AsH3(г) + 3Cl2(г) = AsCl3(г) + 3HCl(г) | |
| 5. | PH3(г) = P(г) + 1,5H2(г) | |
| 6. | MgO(тв) + CO(г) = Mg(тв) + CO2(г) | |
| 7. | CO(г) + Cl2(г) = COCl2(г) | |
| 8. | Cl2O(г) = Cl2(г) + 1,5O2(г) | |
| 9. | 2SO3(г) = 2SO2(г) + O2(г) | |
| 10. | H2S(г) = H2(г) + S(г) | |
| 11. | BaCO3(тв) = BaO(тв) + CO2(г) | |
| 12. | 2HI(г) = H2(г) + I2(г) | |
| 13. | 2HBr(г) = H2(г) + Br2(г) | |
| 14. | 2HCl(г) = H2(г) + Cl2(г) | |
| 15. | 2HF(г) = H2(г) + F2(г) | |
| 16. | FeO(тв) + CO(г) = Fe(тв) + CO2(г) | |
| 17. | H2O(г) + Fe(тв) = H2(г) + FeO(тв) | |
| 18. | H2(г) + S(г) = H2S(г) | |
| 19. | C(тв) + CO2(г) = 2CO(г) | |
| 20. | 2NO2(г) = O2(г) + 2NO(г) | |
| 21. | 0,5N2(г) + 1,5H2(г) = NH3(г) | |
| 22. | Fe2O3(тв) + 3H2(г) = 3Fe(тв) + 3H2O(г) | |
| 23. | Fe3O4(тв) + 4CO(г) = 3Fe(тв) + 4CO2(г) | |
| 24. | PH3(г) = P(г) + 1,5H2(г) | |
| 25. | PbSO4(тв) = PbO(тв) + SO3(г) | |
| 26. | Fe2O3(тв) + 3CO(г) = 2Fe(тв) + 3CO2(г) | |
| 27. | MgCO3(тв) = MgO(тв) + CO2(г) | |
| 28. | 2HI(г) + 0,5O2(г) = I2(г) + H2O(г) | |
| 29. | 2HBr(г) + 0,5O2(г) = Br2(г) + H2O(г) | |
| 30. | 2HCl(г) + 0,5O2(г) = Cl2(г) + H2O(г) |
|
|
Дата добавления: 2014-12-24; Просмотров: 1633; Нарушение авторских прав?; Мы поможем в написании вашей работы!