
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Эфиры серной кислоты. Тиосульфат натрия
|
|
|
|
Тиосерная кислота. Тиосульфат натрия. Получение, свойства, применение.
К эфирам серной кислоты относятся диалкилсульфаты (RO2)SO2. Это высококипящие жидкости; низшие растворимы в воде; в присутствии щелочей образуют спирт и соли серной кислоты. Низшие диалкилсульфаты — алкилирующие агенты.
Диэтилсульфат (C2H5)2SO4. Температура плавления -26°С, температура кипения 210°С, растворим в спиртах, нерастворим в воде. Получен взаимодействием серной кислоты с этанолом. Является этилирующим агентом в органическом синтезе. Проникает через кожу.
Диметилсульфат (CH3)2SO4. Температура плавления -26,8°С, температура кипения 188,5°С. Растворим в спиртах, плохо — в воде. Реагирует с аммиаком в отсутствие растворителя (со взрывом); сульфирует некоторые ароматические соединения, например эфиры фенолов. Получают взаимодействием 60%-ного олеума с метанолом при 150°С, Является метилирующим агентом в органическом синтезе. Канцероген, поражает глаза, кожу, органы дыхания.
Тиосульфат натрия Na2S2O3
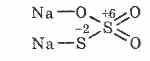
Соль тиосерной кислоты, в которой два атома серы имеют различные степени окисления: +6 и -2. Кристаллическое вещество, хорошо растворимо в воде. Выпускается в виде кристаллогидрата Na2S2O3•5Н2O, в обиходе называемый гипосульфитом. Получают взаимодействием сульфита натрия с серой при кипячении:
Na2SO3+S=Na2S2O3
Как и тиосерная кислота, является сильным восстановителем, Легко окисляется хлором до серной кислоты:
Na2S2O3+4Сl2+5Н2О=2H2SO4+2NaCl+6НСl
На этой реакции было основано применение тиосульфата натрия для поглощения хлора (в первых противогазах).
Несколько иначе происходит окисление тиосульфата натрия слабыми окислителями. При этом образуются соли тетратионовой кислоты, например:
2Na2S2O3+I2=Na2S4O6+2NaI
Тиосульфат натрия является побочным продуктом в производстве NaHSO3, сернистых красителей, при очистке промышленных газов от серы. Применяется для удаления следов хлора после отбеливания тканей, Для извлечения серебра из руд; является фиксажем в фотографии, реактивом в иодометрии, противоядием при отравлении соединениями мышьяка, ртути, противовоспалительным средством.
|
|
|
Тиосерная кислота — неорганическое соединение, двухосновная сильная кислота с формулой H2SO3S. Бесцветная вязкая жидкость, реагирует с водой. Образует соли — неорганические тиосульфаты. Тиосерная кислота содержит два атома серы, один из которых имеет степень окисления +4, а второй — электронейтрален.
Получение
· Реакция сероводорода и триоксида серы в этиловом эфире при низких температурах:

· Действие газообразного хлористого водорода на тиосульфат натрия:
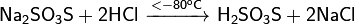
Физические свойства
Тиосерная кислота образует бесцветную вязкую жидкость, не замерзающую даже при очень низкой температуре. Термически неустойчива — разлагается уже при комнатной температуре.
Быстро, но не мгновенно, разлагается в водных растворах. В присутствии серной кислоты разлагается мгновенно.
Химические свойства
· Термически очень неустойчива:
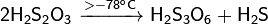
· В присутствии серной кислоты разлагается:
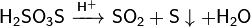
· Реагирует со щелочами:
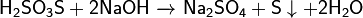
· Реагирует с галогенами:
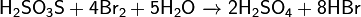
Образует сложные эфиры — органические тиосульфаты.
Тиосульфа́т на́трия (антихлор, гипосульфит, сульфидотриоксосульфат натрия) — Na2S2O3 или Na2SO3S, соль натрия и тиосерной кислоты, образуеткристаллогидрат Na2S2O3·5H2O.
.
Получение
· окислением полисульфидов Na;
· кипячение избытка серы с Na2SO3:
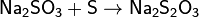
· взаимодействием H2S и SO2 с NaOH (побочный продукт в производстве NaHSO3, сернистых красителей, при очистке промышленных газов от S):
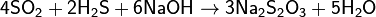
· кипячение избытка серы с гидроксидом натрия:
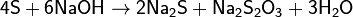
затем по приведённой выше реакции сульфид натрия присоединяет серу, образуя тиосульфат натрия.
|
|
|
Одновременно в ходе этой реакции образуются полисульфиды натрия (они придают раствору жёлтый цвет). Для их разрушения в раствор пропускают SO2.
· чистый безводный тиосульфат натрия можно получить реакцией серы с нитритом натрия в формамиде. Эта реакция количественно протекает (при 80 °C за 30 минут) по уравнению:
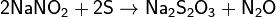
· растворение сульфида натрия в воде в присутствии кислорода воздуха:
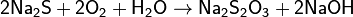
Физические и химические свойства
Бесцветные моноклинные кристаллы. Молярная масса 248,17 г/моль (пентагидрат).
Растворим в воде (41,2 % при 20 оС, 69,86 % при 80оС).
При 48,5 °C кристаллогидрат растворяется в своей кристаллизационной воде, образуя перенасыщенный раствор; обезвоживается около 100оС.
При нагревании до 220 °C распадается по схеме:
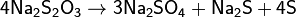
Тиосульфат натрия - сильный восстановитель:
С сильными окислителями, например, свободным хлором, окисляется до сульфатов или серной кислоты:
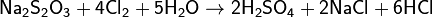
Более слабыми или медленно действующими окислителями, например, иодом, переводится в соли тетратионовой кислоты:
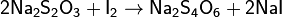
Приведённая реакция очень важна, так как служит основой иодометрии. Следует отметить, что в щелочной среде окисление тиосульфата натрия иодом может идти до сульфата.
Выделить тиосерную кислоту (тиосульфат водорода) реакцией тиосульфата натрия с сильной кислотой невозможно, так как она неустойчива и тут же разлагается:
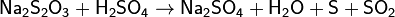
Расплавленный кристаллогидрат Na2S2O3·5H2O очень склонен к переохлаждению.
Применение
· для удаления следов хлора после отбеливания тканей
· для извлечения серебра из руд;
· фиксаж в фотографии;
· реактив в иодометрии
· противоядие при отравлении: As, Br, Hg и другими тяжёлыми металлами, цианидами (переводит их в роданиды) и др.
· для дезинфекции кишечника;
· для лечения чесотки (совместно с соляной кислотой);
· противовоспалительное и противоожоговое средство;
· может использоваться как среда для определения молекулярных весов по понижению точки замерзания (криоскопическая константа 4,26°)
· в пищевой промышленности зарегистрирован в качестве пищевой добавки E539.
· добавки для бетона.
· для очищения тканей от иода
· Марлевые повязки, пропитанные раствором тиосульфатом натрия, использовали для защиты органов дыхания от отравляющего вещества хлора в Первую мировую войну.
|
|
|
|
|
|
|
|
Дата добавления: 2015-08-31; Просмотров: 4432; Нарушение авторских прав?; Мы поможем в написании вашей работы!