
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Абсолютная энтропия идеального кристалла при ОК равна нулю
В идеальном кристалле при О К все частицы находятся в одном энергетическом состоянии, т.к. кристалл упорядочен, тепловое движение
отсутствует, то для идеального кристалла возможно только 1 состояние полной упорядоченности, т.е.
W=1
S=K ln 1=0
Энтропии веществ как и их теплота образования принято относить к
определенным условиям ( и
и 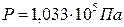 )
)
Энтропию при этих условиях называют стандартной энтропией образования и её значения сведены в таблицу
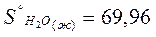 Дж/моль* К Дж/моль* К
|  Дж/моль* К Дж/моль* К
| |
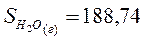 Дж/моль* К Дж/моль* К
| 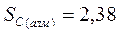 Дж/моль* К Дж/моль* К
|
Энтропия является функцией состояния системы и ее изменения в ходе химических реакций рассчитывается как разница суммарных энтропии продуктов реакций и исходных веществ
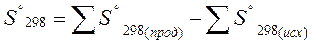 |
Вывод:
Изменение энтропии указывает на термодинамическую вероятность самопроизвольного протекания процесса. Если S > 0, то процесс, наиболее вероятен. S < 0, то процесс менее вероятен, но он может быть осуществлен.
|
|
Дата добавления: 2014-01-15; Просмотров: 621; Нарушение авторских прав?; Мы поможем в написании вашей работы!