
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Складання рівнянь окисно-відновних реакцій
Визначить ступінь окиснення елементів, що входить до складу речовин.
Визначить ступінь окиснення елементів, що входить до складу речовин.
Визначить ступінь окиснення елементів, що входить до складу реагуючих речовин.
Окиснення - це процес, за якого атоми віддають електрони,а відновлення - це процес, за якого атоми приєднують електрони.Процеси віддавання і приєднання електронів відбуваються одночасно: у цьому разі одні сполуки окиснюються, а інші відновлюються.Речовини, у складі яких є атоми, що віддають електрони, називають відновниками, а реагенти, що приймають електрони - окисниками. Окисник, приймаючи електрони, відновлюється, а відновник окиснюється. Кількість електронів, які приймає окисник, дорівнює кількості електронів, які віддає відновник. Процес окиснення супроводжується збільшенням ступеня окиснення, а процес відновлення - зменшенням.
Про окисно-відновні властивості атомів та сполук, що їх містять, можна судити на основі Періодичної системи елементів Д.І.Менделєєва. Відомо, що за номером групи можна визначити як найнижчий так і найвищий ступінь окиснення. Наприклад, елемент Сульфур знаходиться у шостій групі Періодичної системи. Номер групи показує, що атом Сульфуру має найвищий ступінь окиснення +6, а найнижчий -2. Відомі також сполуки, як сульфатна кислота H2SO4 та її солі, в яких атом сірки має проміжний ступінь окиснення +4. Атоми в проміжному ступені окиснення можуть бути як окисниками так і відновниками одночасно.
До найважливіших відновників належать: метали, гідроген, вугілля, СО, Н2S, SO2, H2SO3, HJ, HB, HCl, ZnCl2, MnSO4, CrCl3, NH3, N2H4, NO, H3PO3, альдегіди, спирти, мурашина та щавлева кислоти, глюкоза.
До найактивніших окисників відносять: KnMnO4, K2CrO4, O2, O3, H2SO3 (конц), Н2О2, HNO3, Ag2О, РвО2, галогени, йони Аu3+, Ag+, (NH4)2S2O8, гіпохлорити NaClO, царська водка.
Правильно складене рівняння реакції є виразом закону збереження маси речовини. Це означає, що число одних і тих самих атомів у вихідних речовинах та продуктах реакції повинно бути однаковим. Повинні зберігатися і заряди: сума зарядів вихідних речовин завжди повинна дорівнювати сумі зарядів продуктів реакції.
При складанні рівнянь необхідно додержуватись певного порядку:
1. проставити над елементами у речовинах ступені окиснення і визначити, що є окисником, а що відновником. Якщо у рівнянні відсутня права частина, тобто не записані продукти реакції, треба їх дописати, виходячи із можливих варіантів зміни ступенів окиснення окисника і відновника;
2. скласти схему йонно-електронного балансу, тобто виписати елементи окисника і відновника і написати напівреакції їх окиснення і відновлення;
3. знайти найменше спільне кратне число електронів, що приймають участь в окисно-відновному процесі, та визначити коефіцієнти, які повинні стояти у рівнянні перед речовинами, що змінили ступені окиснення;
4. підібрати коефіцієнти для речовин, в яких не відбулося змін ступеню окиснення;
5. перевірити правильність запису рівняння, підрахувавши кількість атомів у лівій та правій частинах рівняння - вони повинні бути однаковими.
Найчастіше при складанні ОВР використовують метод електронного балансу та йонно-електронний метод (або метод напівреакцій). Вказані методи ґрунтуються на положенні, що в окисно-відновних процесах загальна кількість електронів, які віддає відновник, дорівнює загальній кількості електронів, які приєднує окисник.
При складанні рівнянь окисно-відновних процесів найчастіше використовується метод електронного балансу, що полягає у визначенні кількості електронів, які переміщуються від відновника до окисника і зрівнянні їх загальної кількості.
Розглянемо послідовність етапів складання рівнянь за методом електронного балансу:
1. записують у молекулярному вигляді вихідні речовини і продукти реакції, Наприклад:
KMnO4 + HCI→KCI + MnCI2 +CI2 +H2O;
2. зазначають ступені окиснення атомів, які їх змінили:
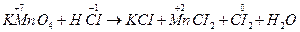 ;
;
3. записують електронні рівняння процесів окиснення і відновлення (баланс електронного обміну):
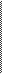
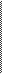
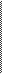
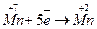 5 2 Відновлення
5 2 Відновлення
 2 5 Окиснення
2 5 Окиснення
З урахуванням того, що кількість відданих відновником електронів повинна дорівнювати кількості електронів, приєднаних окисником, знаходять спільний множник для двох електронно-йонних рівнянь. Ці множники підбирають за правилом знаходження найменшого спільного кратного, у нашому прикладі таким спільним множником буде 10. Отже, множники 2 і 5 є коефіцієнтами відповідно, біля йонів Мангану і Хлору в рівнянні окисно-відновної реакції.
Якщо біля атому елементу є індекс (наприклад, хлор СІ2), то його враховують, і коефіцієнт ставлять спочатку перед цією речовиною.
Якщо один і той же елемент і змінює, і не змінює ступінь окиснення, то спочатку коефіцієнт ставлять там, де ступінь окиснення змінився:
KMnO4 + HCI→KCI + 2MnCI2 +5CI2 +H2O;
4. урівнюють кількість атомів металів, неметалів, кислотних залишків, Гідрогену, які не змінили ступеню окиснення; стрілку в рівняння замінюють на знак рівності:
2KMnO4 + 16HCI = 2KCI + 2MnCI2 +5CI2 + 8H2O;
5. правильність підбору коефіцієнтів перевіряють за кількістю атомів Оксигену: 2 · 4 = 8.
У тих випадках, коли кількість елементів, що змінюють ступінь окиснення більше, ніж 2, визначають загальну кількість електронів, яку віддав відновник, чи загальну кількість електронів, яку приймає окисник, і надалі продовжують аналогічно. Наприклад:
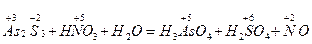
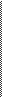
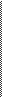
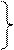
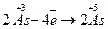 28 3
28 3
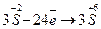 84
84
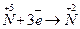 3 28
3 28
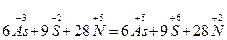 або
або

Йонно-електронний метод, або метод напівреакцій, відображає сутність ОВР, які відбуваються у розчинах електролітів і ґрунтуються на складанні напівреакцій процесів окиснення й відновлення з наступним підсумовуванням їх у загальне окисно-відновне рівняння. У разі складання рівнянь цим методом необхідно пам’ятати наступні правила:
1. записують в йонному вигляді відновник, окисник та продукти їх окиснення та відновлення. Сильні електроліти записують у вигляді йонів, наприклад, SO42-, NO3-, NO2-, SO32-, CIO4-, CI-, Fe3+. Слабкі електроліти, осади та гази, позначають у вигляді молекул: H2O, SO2, SO3, CO2, NH3, H2, NO2, Fe2O3, Ag2O, Cu2S;
2. якщо вихідна речовина містить більше атомів Оксигену, ніж продукти реакції, то вивільнений Оксиген зв’язується в кислих розчинах йонами гідрогену Н+ з утворенням води, а в нейтральних та лужних – у гідроксид-йони;
3. якщо вихідна речовина містить менше атомів Оксигену, ніж продукт реакції, то їхня нестача компенсується в кислих та нейтральних розчинах молекулами води, а лужних – гідроксид йонами;
4. сумарна кількість та знак електричних зарядів у лівій і правій частині рівняння мають бути однаковими;
5. у разі підсумовування йонно-електронних рівнянь можна переносити члени рівняння з одного боку в інший, додавати однакові доданки в кожну частину рівняння. Наприклад, розглянемо реакцію взаємодії калій перманганату KMnO4 з калій йодидом КІ у кислому середовищі:

Запишемо окисно-відновне рівняння в скороченій йонно-молекулярній формі, відображаючи сильні електроліти у вигляді йонів, а слабкі у вигляді молекул. Ті йони, що не змінюють ступінь окиснення, не зазначають:
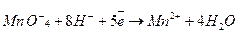
Напівреакція окиснення йодид-йона до йоду буде такою:
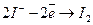
Щоб зрівняти кількість електронів, які беруть участь у напівреакціях окиснення та відновлення, потрібно напівреакцію окиснення помножити на 5, а напівреакцію відновлення на 2:
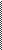
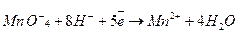 2
2
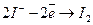 5
5
Підсумувавши почленно ці напівреакції, одержимо
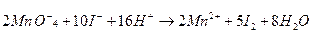
Якщо рівняння реакції складене правильно, то сумарний заряд усіх йонів у правій та лівій частинах рівняння повинен бути однаковим. Для написання молекулярного рівняння в лівій частині до кожного катіона та аніона підбирають відповідні аніони та катіони, а потім записують ці ж йони в такій же кількості у праву частину рівняння:
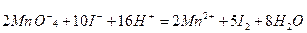
2К+ + 10K+ +8SO42-=2SO42-+ 12K++6SO42-
Після об`єднання цих йонів у молекули отримують молекулярне рівняння:
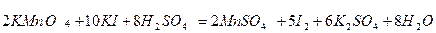
|
|
Дата добавления: 2014-11-25; Просмотров: 1658; Нарушение авторских прав?; Мы поможем в написании вашей работы!