
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Пятичленные гетероциклические соединения с одним гетероатомом
|
|
|
|
Теория
Этапы занятий и контроль усвоения знаний
Вопросы для самоподготовки
1. Напишите структурные формулы 2.5-диметилфурана, 2-аминопиридина,
3-оксииндола, 2,6-диоксипиримидина; 2,6,8-триоксипурина.
2. Получите из пиридина никотиновую кислоту. Напишите уравнение реакции ее с
NH3.
3. Почему мочевая кислота проявляет кислотные свойства?
4. Напишите формулы пиримидиновых и пуриновых оснований, входящих в состав
нуклеиновых кислот.
| Этапы занятия | Формы проведения этапа | Время, мин |
| 1. Проверка выполнения домашнего задания. | Проверка преподавателем выполнения домашнего задания в рабочей тетради. | |
| 2. Контроль самоподготовки. | Тест-контроль по теме занятия и оценка его результатов (0, 5, 10 баллов) | |
| 3. Разбор теоретического материала. | Устный опрос студентов у доски, объяснение наиболее трудных вопросов преподавателем. | 150 |
Содержание этапов занятия
1-й этап. Преподаватель проверяет наличие выполненного домашнего задания в рабочих тетрадях и оценивает его по пятибалльной системе.
2-й этап. Студент письменно отвечает на билет программированного контроля. Ответ оценивается по принятой балльной системе (0, 5, 10 баллов).
3-й этап. На 1 занятии по теме «Гетероциклические соединения» студенты учатся писать формулы пяти- и шестичленных гетероциклов с одним гетероатомом. Разбирают электронное строение «пиррольного» и «пиридинового» атомов азота, рассматривают свойства, характерные для этих соединений: ароматичность, кислотно-основные, нуклеофильные.
На 2 занятии рассматриваются пяти- и шестичленные гетероциклические соединения с двумя гетероатомами: имидазол, пиразол, пиримидин, окси- и аминопрозводные пиримидина – урацил, тимин, цитозин в лактимной и лактамной формах; конденсированные гетероциклические соединения: индол, пурин, окси- и аминопроизводные пурина – аденин, гуанин, мочевая кислота в лактимной и лактамной форме; разбирается строение нуклеозидов, нуклеотидов, фрагментов полинуклеотидной цепи.
|
|
|
 | |||||
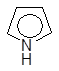 | |||||
 | |||||
фуран пиррол тиофен
Все эти соединения являются ароматическими, так как отвечают критериям
ароматичности:
1) Sr2 – гибридизованные атомы пиррола, фурана, тиофена образуют плоский
s- скелет;
2) количество р- электронов удовлетворяет формуле Хюккеля 4n+2=N, где n-целое
натуральное число.
4р Электрона поставляют атомы углерода и 2р- электрона – гетероатомы N, O или S. Образуется p- электронный секстет;
3) 6р- электронов образуют единое сопряженное облако, делокализованное по всему кольцу.
Общей чертой ароматических гетероциклов и производных бензола является
высокая термодинамическая устойчивость.
Отличие от бензола.
1) 6р Электронов распределяются по пятицентровой системе, поэтому такие системы называются суперароматическими, или p-избыточными; их реакции электрофильного замещения идут легче, чем в бензоле.
2) Из-за влияния гетероатома электронная плотность увеличена в a-положениях кольца (2 и 5), поэтому атака электрофильного реагента происходит предпочтительно в эти положения.
3) Энергия сопряжения у пятичленных гетероциклических соединений меньше, чем у бензола (22-28 ккал/моль, а у бензола– 36 ккал/моль).
Поэтому легче идут реакции с раскрытием кольца. Например, реакции восстановления.
Электронное строение «пиррольного» атома азота
 |

a a
Химические свойства пятичленных гетероциклических соединений на примере пиррола.
1. Ароматические свойства. Реакция SЕ протекает легче, в более мягких условиях.
|
|
|

SO2Cl2

 + SO2 + HCl
+ SO2 + HCl
a-хлорпиррол
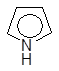 |

SO3
 в пиридине
в пиридине

a- сульфопиррол
2. Основные свойства почти отсутствуют, так как электронная пара втянута в сопряжение: Коснпиррола=10-14; Косн анилина =10-10. При насильственном протонировании сильными минеральными кислотами ароматическая система нарушается, пиррол превращается в неустойчивый дивиниламин, который быстро полимеризуется с образованием смолы:
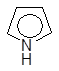
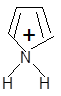 Н+ полимеризация
Н+ полимеризация

 смола
смола
неустойчивый
дивинилимин
Это свойство осмоляться под действием кислот называется «ацидофобностью», и его надо учитывать при выборе реагентов в реакциях электрофильного замещения (см. п.1)
3. Кислотные свойства – тоже слабые. Взаимодействие со щелочными металлами идет с образованием неустойчивых солей.
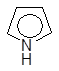
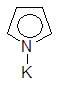 К/t
К/t

 + Н2
+ Н2
Н2О
неустойчивая соль
пирролят калия
4. Восстановление (HI, t=30°). Протекает легче из-за меньшей энергии сопряжения по сравнению с бензолом.
2[H] 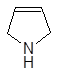
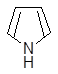
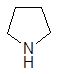 2[H]
2[H]
 |  |
пиррол пирролин пирролидин
По мере восстановления основность повышается. Восстановленное пиррольное кольцо входит в состав алкалоидов, аминокислот (пролин, оксипролин). Его производное – N-винилпирролидон применяется в медицине в качестве заменителя плазмы крови и клеящего, связующего материала.
 |
В природных соединениях ароматический пиррольный цикл часто встречается в различных многоядерных системах, из которых особенно важно ароматическое порфириновое ядро, входящее в состав гемоглобина и хлорофилла. Порфирин имеет единое p- электронное облако, содержащее 26 p- электронов; 22 электрона одиннадцати сопряженных двойных связей и 2 неподеленные пары электронов атома азота. Этот цикл отличается также высокой термодинамической устойчивостью.
|
|
|
|
|
Дата добавления: 2014-11-25; Просмотров: 622; Нарушение авторских прав?; Мы поможем в написании вашей работы!