
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Рецептор и аденилатциклаза - это отдельные белки, которые функционально взаимодействуют в
|
|
|
|
12-16
12-12
12.2.2. Стероидные гормоны часто вызывают и первичный, и вторичный ответ [7]
Во многих случаях реакция на стероидный гормон бывает двухстадийной. Прямая индукция транскрипции нескольких специфических генов называется первичным ответом. Затем продукты этих генов могут в свою очередь активировать другие гены и вызвать через некоторое время вторичный ответ. Таким образом, простой гормональный пусковой сигнал способен производить весьма сложные изменения в картине экспрессии генов.
Поразительный пример мы находим у плодовой мушки дрозофилы. Уже спустя 5-10 мин после инъекции стероидного гормона линьки-
экдизона –в гигантских политенных хромосомах слюнных желез появляются шесть новых участков интенсивного синтеза РНК (они имеют вид пуфов; см. разд. 9.2.6). Через определенное время некоторые из белков, синтезированных во время первичного ответа, индуцируют синтез РНК еще примерно в сотне новых участков, что приводит к появлению
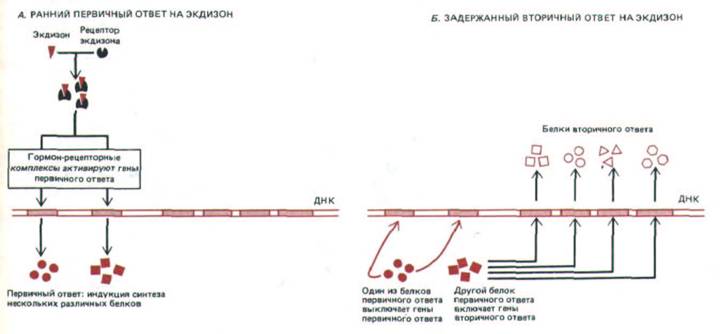
Рис. 12-11. Схема раннего первичного (А) и задержанного вторичного (Б) ответа клеток дрозофилы на экдизон. Некоторые из белков, синтезируемых при первичном ответе, включают гены, ответственные за вторичный ответ, а другие выключают гены, участвовавшие в первичном ответе. На самом деле в обоих ответах участвует больше генов, чем показано на схеме.
Албертс Б., Брей Д., Льюис Дж., Рэфф М., Робертс К. Уотсон Дж. Д. Молекулярная биология клетки: В 3-х т. 2-е изд. перераб. и доп. Т. 2.: Пер. с англ. – М.: Мир, 1993. – 539 с.
большой группы белков, характерных для вторичного ответа. Один или несколько первичных белков управляют всем ответом, выключая по принципу обратной связи транскрипцию всех генов, участвовавших в первичном ответе (рис. 12-11). Вполне вероятно, что аналогичные механизмы осуществляют усиление и регуляцию многих реакций на гормоны и в клетках млекопитающих.
|
|
|
12.2.3. В разных клетках-мишенях стероидные гормоны регулируют активность разных генов [8]
Реакция на стероидные гормоны, как и на гормоны вообще, определяется не только природой гормона, но в не меньшей степени и природой клетки-мишени (см. рис. 12-5). В принципе этому может быть два объяснения: либо разные типы клеток имеют разные рецепторы для одного и того же гормона, либо рецепторы одинаковы, но они активируют разные гены. Имеющиеся данные говорят в пользу второго объяснения.
Такие данные были получены в молекулярногенетических экспериментах, показавших, что рецепторные белки для эстрадиола, кортизола и прогестерона кодируются каждый своим собственным единичным геном, и при изучении мутантов млекопитающих с дефектным рецептором мужского полового гормона тестостерона. Все млекопитающие, не подвергшиеся в эмбриональном периоде воздействию тестостерона, развиваются по женскому пути. Мутантные генетические самцы имеют нормальные семенники, вырабатывающие тестостерон, но ткани этих самцов не реагируют на гормон из-за дефектности соответствующих рецепторов. Поэтому у таких самцов развиваются все вторичные половые признаки самок, и семенники их не опускаются в мошонку, а остаются в брюшной полости. Этот синдром тестикулярной феминизации встречается у мышей, крыс, крупного рогатого скота, а также у человека. Хотя изменен только ген, кодирующий рецептор тестостерона, затронутыми оказываются все разнообразные типы клеток, в норме реагирующих на этот гормон (рис. 12-12).
Почему в клетках разного типа один и тот же стероидный гормон активирует разные группы генов? Как описано в гл. 10, для активации эукариотического гена нужно, чтобы с ним, как правило, связалось несколько регуляторних белков (разд. 10.1.5). Поэтому рецептор сте-
|
|
|
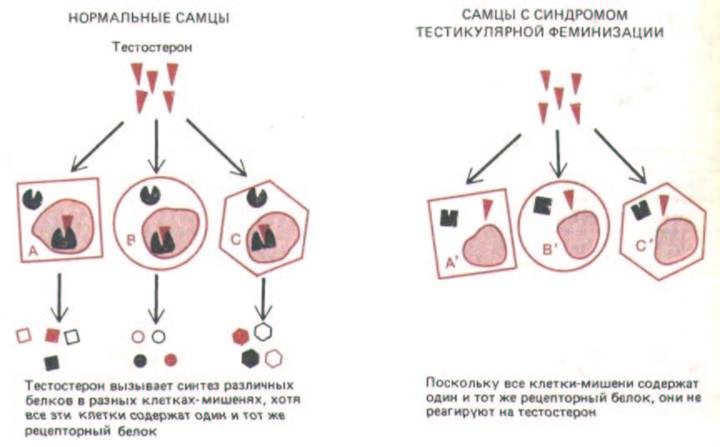
Рис. 12-12. Различные клетки-мишени по-разному реагируют на тестостерон, хотя содержат одинаковые рецепторные белки. При синдроме тестикулярною феминизации мутация в одном-единственном гене, изменяющая рецептор тестостерона, приводит к тому, что все клетки-
мишени теряют способность реагировать на этот гормон.
Албертс Б., Брей Д., Льюис Дж., Рэфф М., Робертс К. Уотсон Дж. Д. Молекулярная биология клетки: В 3-х т. 2-е изд. перераб. и доп. Т. 2.: Пер. с англ. – М.: Мир, 1993. – 539 с.
роидного гормона может активировать ген только в присутствии необходимой комбинации регуляторных белков, причем некоторые из этих белков тканеспецифичны.
Таким образом, каждый стероидный гормон вызывает характерный комплекс ответов, так как 1) рецепторы для данного гормона имеются только в клетках определенных типов и 2) клетки каждого из этих типов содержат различные комбинации других тканеспецифичных регуляторных белков, которые совместно с активированным стероидным рецептором влияют на транскрипцию специфических групп генов.
Заключение
Стероидные гормоны - это небольшие гидрофобные молекулы, производные холестерола. В крови они находятся в форме
водорастворимого комплекса со специальным белком-переносчиком. Освободившись от переносчика, они диффундируют через плазматическую
мембрану клетки-мишени и обратимо связываются в цитоплазме или в ядре со специфическими белками-рецепторами. Присоединив к себе гормон, рецептор приобретает повышенное сродство к определенным последовательностям ДНК, которые начинают действовать как энхансеры, т. е.
стимулируют транскрипцию нескольких соседних генов. Продукты некоторых из этих генов могут в свою очередь активировать другие гены и
вызывать более поздний вторичный ответ, усиливая таким образом действие гормона. Каждый стероидный гормон узнается своим особым
рецептором-представителем группы гомологичных белков. Один и тот же рецептор в разных клетках-мишенях регулирует разные наборы генов, вероятно потому, что для транскрипции специфических генов нужны также и другие связывающиеся с ДНК белки, которые в разных клетках
|
|
|
различны.
12.3. Механизмы передачи сигнала с участием рецепторних белков клеточной поверхности [9]
Все водорастворимые сигнальные молекулы (в том числе нейромедиаторы, пептидные гормоны и факторы роста), как, впрочем, и некоторые жирорастворимые, присоединяются к специфическим белковым рецепторам на поверхности клеток-мишеней. Поверхностные рецепторы связывают сигнальную молекулу (лиганд) с высоким сродством, и это внеклеточное событие порождает внутриклеточный сигнал, изменяющий поведение клетки.
Используя лиганды, меченные радиоактивными атомами, флуоресцентными красителями или электроноплотными частицами (типа коллоидного золота), можно изучать распределение рецепторов на поверхности клетки. Было показано, что число рецепторов для конкретного лиганда может варьировать в пределах от 500 до более чем 100000 на клетку и что они либо располагаются на мембране случайным образом, либо сосредоточены в определенных ее участках. Подобно другим мембранным белкам, рецепторы клеточной поверхности с трудом поддаются выделению в чистом виде и изучению, особенно в связи с тем, что они составляют менее 0,1% общей массы белка плазматической мембраны.
Методы клонирования последовательностей ДНК, кодирующих поверхностные рецепторы, и здесь позволили преодолеть многие трудности и в корне изменили наши представления о структуре и функциях рецепторов.
В отличие от внутриклеточных рецепторов для стероидных и тиреоидных гормонов, рецепторы клеточной поверхности не регулируют
Албертс Б., Брей Д., Льюис Дж., Рэфф М., Робертс К. Уотсон Дж. Д. Молекулярная биология клетки: В 3-х т. 2-е изд. перераб. и доп. Т. 2.: Пер. с англ. – М.: Мир, 1993. – 539 с.
непосредственно экспрессию генов. Они лишь передают сигнал через плазматическую мембрану, а влияние, которое они оказывают на процессы в цитозоле или в ядре, связано с образованием новых внутриклеточных сигналов. Можно было бы подумать, что рецепторы клеточной поверхности просто переносят внешние сигнальные молекулы через мембрану в цитозоль, превращая их во внутриклеточный сигнал, однако это не так. Правда, многие белковые сигнальные молекулы, например инсулин, действительно поглощаются клеткой путем эндоцитоза при участии рецептора (разд.
|
|
|
12.5.1), но они не выходят из эндосомных или лизосомных пузырьков в цитозоль. По-видимому, задача внешнего лиганда сводится к тому, чтобы вызвать конформационное изменение белка-рецептора, находящегося на поверхности клетки. В самом деле, действие нормального лиганда нередко могут имитировать связывающиеся с рецептором антитела; этот феномен лежит в основе ряда патологических состояний. Например, весьма обычной причиной гипертиреоза - избыточной функции щитовидной железы - у человека бывает аномальная выработка антител, присоединяющихся к рецепторам тиреотропного гормона; рецепторы при этом активируются и вызывают гиперфункцию железы.
В этом разделе мы рассмотрим, как конформационное изменение белкового рецептора на клеточной поверхности, вызванное присоединением внеклеточного лиганда, позволяет рецептору прямо или косвенно превращать внешний сигнал в сигнал, действующий внутри клетки.
12.3.1. Известны по меньшей мере три класса белковых рецепторов клеточной поверхности: образующие канал, сопряженные с G-белками и каталитические [9]
Большинство белковых рецепторов клеточной поверхности можно отнести к одному из трех классов в зависимости от механизма, используемого для передачи сигнала. Каналообразующие рецепторы - это регулируемые медиаторами ионные каналы, участвующие главным образом в быстрой синаптической передаче сигналов между электрически возбудимыми клетками. Для управления такого рода каналами используется небольшое число нейромедиаторов, которые на короткое время открывают или закрывают образуемый рецепторами канал, изменяя таким образом ионную проницаемость плазматической мембраны, а тем самым и возбудимость постсинаптической клетки. Изучение последовательностей ДНК, кодирующих эти рецепторы, показало, что они относятся к одному семейству гомологичных белков, насквозь пронизывающих мембрану. Эти рецепторы обсуждаются в гл. 19 (разд. 19.3) и здесь рассматриваться не будут.
Каталитические рецепторы при активации лигандом начинают работать как ферменты. Большинство известных каталитических рецепторов - трансмембранные белки с цитоплазматическим доменом, обладающим тирозин-специфической протеинкиназной активностью.
Рецепторы, сопряженные с G-белками, опосредованно активируют или ингибируют определенные ферменты или ионные каналы, связанные с плазматической мембраной. Взаимодействие между рецептором и ферментом или ионным каналом происходит через третий белок, который называют GTP-связывающим регуляторным белком (или G-белком). Рецепторы, связанные с G-белком, обычно запускают целую цепь событий, изменяющих концентрацию одного или нескольких малых внутриклеточных сигнальных молекул, часто называемых внутриклеточными
посредниками или внутриклеточными медиаторами. Эти молекулы в свою очередь действуют, изменяя поведение других белков-мишеней в клетке. Два наиболее важных посредника-это циклический AMP (cAMP) и
Албертс Б., Брей Д., Льюис Дж., Рэфф М., Робертс К. Уотсон Дж. Д. Молекулярная биология клетки: В 3-х т. 2-е изд. перераб. и доп. Т. 2.: Пер. с англ. – М.: Мир, 1993. – 539 с.
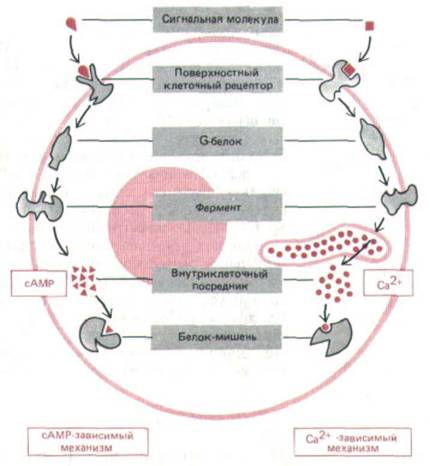
Рис. 12-13. Два главных механизма, с помощью которых рецепторы клеточной поверхности, сопряженные с G-белками, запускают образование внутриклеточных посредников. В обоих вариантах связывание внеклеточного лнганда изменяет конформацию цитоплазматического домена рецептора так, что он связывается с G-белком, который затем активирует (или ингибирует) определенный фермент плазматической мембраны. В некоторых случаях G-белок взаимодействует не с ферментом, а с ионным каналом. В сАМР-пути активируемый Gs-белком фермент синтезирует циклический AMP. В Са2 + -пути с помощью фермента образуется растворимый посредник, который освобождает из внутриклеточных хранилищ ионы Са 2+. И сАМР, и Са2+ связываются в клетке с другими специфическими белками, изменяя их активность.
Са2 +. Передаваемые ими сигналы генерируются разными путями (те и другие с участием G-белков) и используются во всех животных клетках (см.
рис. 12-13). Мы рассмотрим эти пути, прежде чем вернемся к каталитическим рецепторам с тирозин-специфической протеинкиназной активностью;
начнем с экспериментов, которые привели к открытию сАМР и проложили путь к нынешнему пониманию того, каким образом внутриклеточные посредники появляются в ответ на внеклеточный сигнал.
12.3.2. Циклический AMP-вездесущий посредник в животных клетках [10]
В клетках мышц или печени воздействие адреналина стимулирует расщепление запасов гликогена. Оказалось, что адреналин активирует
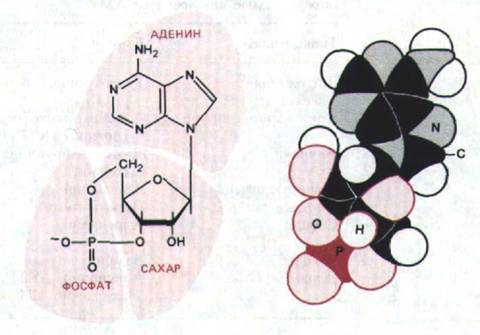
Рис. 12-14. Структурная формула и объемная модель циклического AMP (С, Н, N, О и Р-атомы углерода, водорода, азота, кислорода и фосфора соответственно).
Албертс Б., Брей Д., Льюис Дж., Рэфф М., Робертс К. Уотсон Дж. Д. Молекулярная биология клетки: В 3-х т. 2-е изд. перераб. и доп. Т. 2.: Пер. с англ. – М.: Мир, 1993. – 539 с.
фермент гликогенфосфорилазу, катализирующий это расщепление. Далее удалось выяснить, что обработка изолированных мембран печеночных клеток адреналином (в присутствии АТР) вызывает образование низкомолекулярного термостабильного фактора, способного заменять гормон и активировать фосфорилазу в экстракте тех же клеток, не содержащем мембран. В 1959 г. этот медиатор был идентифицирован как циклический AMP (cAMP, рис. 12-14), который, как было позже установлено, регулирует многие внутриклеточные реакции во всех до сих пор изученных прокариотических и животных клетках.
Идентификация циклического AMP привела к изучению ферментов, участвующих в его синтезе и разрушении. Чтобы сАМР мог служить внутриклеточным посредником, его концентрация в клетке (обычно ≤ 10-6 М) должна быть подвержена быстрым изменениям в ту и другую сторону под действием определенных внеклеточных сигналов (при гормональной стимуляции она может за несколько секунд увеличиться в 5 раз). Как мы увидим (разд. 12.4.7), для этого быстрый синтез молекул должен уравновешиваться быстрым их расщеплением или удалением. Циклический AMP синтезируется из АТР ферментом аденилатциклазой, связанным с плазматической мембраной клетки, но быстро расщепляется одним или несколькими ферментами - сАМР-фосфодиэстеразами, которые гидролизуют его до аденозин-5'-монофосфата (5'-АМР) (рис. 12-15).
|
|
|
|
|
Дата добавления: 2015-08-31; Просмотров: 827; Нарушение авторских прав?; Мы поможем в написании вашей работы!