
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Табличное значение стандартной энтальпии сгорания н-пропана
|
|
|
|
Реакция горения в воздухе
Расчет термодинамических величие
Физико-химические свойства
Москва 2016
Пропан- бесцветный газ без запаха. Очень мало растворим в воде. Точка кипения −42,1 °C. Точка замерзания −188 °C. Образует с воздухом взрывоопасные смеси при концентрации паров от 2,1 до 9,5 %. Температура самовоспламенения пропана в воздухе при давлении 0,1 МПа (760 мм рт. ст.) составляет 466 °С. Критическая температура пропана Tкр = 370 К, критическое давление Pкр = 4,27 МПа, критический удельный объем Vкр = 0,00444 м3/кг[5] Плотность сжиженного пропана при 298 K — 0,493 кг/л.
· Плотность газовой фазы при нормальных условиях = 2,019 кг/м3.
· Плотность газовой фазы при температуре 15°С = 1,900 кг/м3.
· Удельная теплота сгорания = 48 МДж/кг.
В химической промышленности используется для получения пропилена, сырья для производства полипропилена.
Является исходным сырьём для производства растворителей.
Используется как пропилен.
В пищевой промышленности пропан зарегистрирован в качестве В химической промышленности используется для получения пропилена, сырья для производства полипропилена.
Является исходным сырьём для производства растворителей.
Используется как пропеллент.
В пищевой промышленности пропан зарегистрирован в качестве пищевой добавки E944.
E944.
С n Н m O r + 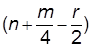 ×(O2 + 3,75 N2)
×(O2 + 3,75 N2) 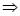
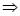 n CO2(г) +
n CO2(г) + 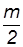 H2O(ж) +
H2O(ж) + 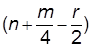 ×3,75 N2.
×3,75 N2.
н- 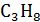 : n =3, m =8, r =0:
: n =3, m =8, r =0:
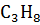 (г) +5 (O2 + 3,75N2)
(г) +5 (O2 + 3,75N2) 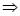 3CO2(г) + 4H2O(ж) + 18,75N2.
3CO2(г) + 4H2O(ж) + 18,75N2.
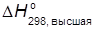
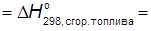 -2219,7 кдж кДж/моль. н-
-2219,7 кдж кДж/моль. н- 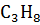
2.3. Высшая теплота сгорания топлива QВ:
Qв 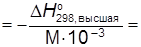
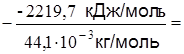 50333,33кДж/кг СН4 ≈
50333,33кДж/кг СН4 ≈
≈50,3МДж/кг н- 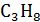 .
.
2.4. Низшая энтальпия сгорания топлива 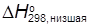 рассчитывается по уравнению реакции:
рассчитывается по уравнению реакции:
С n Н m O r + 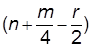 ×(O2 + 3,75 N2)
×(O2 + 3,75 N2) 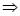
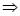 n CO2(г) +
n CO2(г) + 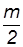 H2O(ж) +
H2O(ж) + 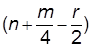 ×3,75 N2.
×3,75 N2.
н- 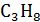 : n =3, m =8, r =0:
: n =3, m =8, r =0:
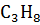 (г) +5 (O2 + 3,75N2)
(г) +5 (O2 + 3,75N2) 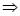 3CO2(г) + 4H2O(ж) + 18,75N2.
3CO2(г) + 4H2O(ж) + 18,75N2.
|
|
|
Низшая энтальпия сгорания 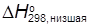 отличается от высшей на энтальпию конденсации водяного пара
отличается от высшей на энтальпию конденсации водяного пара 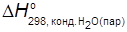 =−44,01 кДж/моль. Из уравнения реакции горения пропана видно, что образуется четыре моля воды. Поэтому
=−44,01 кДж/моль. Из уравнения реакции горения пропана видно, что образуется четыре моля воды. Поэтому
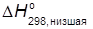
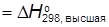 –
– 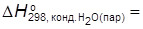 −2219,7 +2∙44,01=
−2219,7 +2∙44,01=
=-2131,68 кДж/моль.
2.5. Низшая теплота сгорания топлива QН:
QH 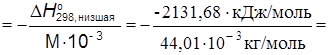 48436,26 кДж/кг СН4 ≈
48436,26 кДж/кг СН4 ≈
≈48,2 МДж/ кг С3Н8.
2.6. Теоретически необходимое количество воздуха для полного сгорания 1 кг Пропана:
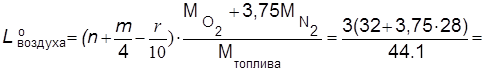
=4,71 кг воздуха/кг топлива
2.7. Количество топливовоздушной смеси:
М1 = 1топлива + 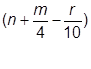 (О2 + 3,75N2)=1+5(1+3,75)=24,75 моль.
(О2 + 3,75N2)=1+5(1+3,75)=24,75 моль.
2.8. Низшая теплота сгорания топливовоздушной смеси q н, она же калорийность стехиометрической смеси топлива с воздухом:
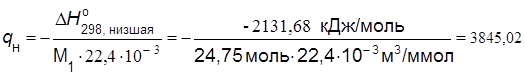 кДж/м3.
кДж/м3.
Таблица 5
Сравнительные характеристики (QН,  , q н)
, q н)
|
|
|
|
Дата добавления: 2017-01-13; Просмотров: 1481; Нарушение авторских прав?; Мы поможем в написании вашей работы!