
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Силы, обеспечивающие ионную и ковалентную связи, называются химическими. Эти силы убывают с возрастанием расстояния между атомами
Межмолекулярные силы.
Но между нейтральными атомами и молекулами действуют еще и дальнодействующие силы притяжения. Они обусловлены кулоновским взаимодействием заряженных частиц, входящих в состав нейтральных атомов и молекул на расстояниях, значительно превосходящих размеры молекул. К ним относят силы, возникающие при взаимодействии
- постоянных дипольных моментов атомов или молекул (диполь – дипольное взаимодействие)
- постоянных диполей с диполями индуцированными (индукционное взаимодействие),
- между мгновенными диполями (дисперсионное взаимодействие) (силы Ван-дер-Ваальса).
Диполь – дипольное (ориентационное) взаимодействие является наиболее сильным, оно возникает при сближении двух полярных молекул. Минимальная энергия взаимодействия соответствует ориентации, при которой положительный полюс одной молекулы соседствует отрицательным полюсом другой. В газах и жидкостях ориентации полярных молекул препятствует тепловое движение.
Энергия диполь – дипольного взаимодействия
 ~
~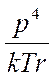 ,
,
где  - дипольный момент молекулы,
- дипольный момент молекулы,  - температура,
- температура,  - расстояние между центрами диполей.
- расстояние между центрами диполей.
Полярная молекула создает электрическое поле, которое поляризует неполярную молекулу – индуцирует в ней дипольный момент. Потенциальная энергия индукционного взаимодействия
 ~
~ 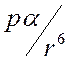 ,
,
где 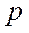 - дипольный момент полярной молекулы,
- дипольный момент полярной молекулы, 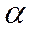 - поляризуемость молекулы,
- поляризуемость молекулы, 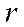 - межмолекулярное расстояние.
- межмолекулярное расстояние.
Дисперсионное взаимодействие в чистом виде проявляется у инертных газов. У неполярных молекул дипольное взаимодействие возникает следующим образом – вследствие движения электронов в атомах возникают мгновенные дипольные моменты, отличные от нуля.
Дисперсионное взаимодействие связано с наличием у невозбужденных атомов или молекул нулевых колебаний, не зависящих от температуры.
Предположим, что колебания электронов происходят вдоль прямой, соединяющей атомы. При отклонении электронов от положения равновесия на  и
и  у атомов появляются дипольные моменты
у атомов появляются дипольные моменты  и
и  . Потенциальная энергия взаимодействия диполей будет
. Потенциальная энергия взаимодействия диполей будет
 ,
,
где 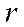 - расстояние между диполями. Из этого выражения видно, что
- расстояние между диполями. Из этого выражения видно, что  , значит, атомы притягиваются друг к другу.
, значит, атомы притягиваются друг к другу.
Для диполя в постоянном электрическом поле дипольный момент
 .
.
где  - поляризуемость атома.
- поляризуемость атома.
Для гармонического осциллятора сила, действующая на заряд равна  , и при равновесии
, и при равновесии
 , откуда
, откуда  .
.
В результате получается
 .
.
Для реальных атомов
 ,
,
где  - энергия ионизации атома,
- энергия ионизации атома, 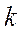 - коэффициент порядка единицы.
- коэффициент порядка единицы.
К молекулярным силам относятся также силы отталкивания. Возникновение этих сил связано с тем, что при достаточном сближении происходит соприкосновение электронных оболочек частиц. Дальнейшее сближение невозможно, т.к. это приведет к взаимному проникновению электронных оболочек, что запрещено принципом Паули. Силы отталкивания являются короткодействующими и быстро убывают с увеличением расстояния между атомами и молекулами. Точно рассчитать  для межмолекулярного отталкивания невозможно. Обычно пользуются формулой Ленарда-Джонса:
для межмолекулярного отталкивания невозможно. Обычно пользуются формулой Ленарда-Джонса:
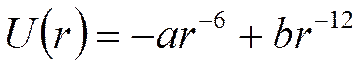 ,
,
где параметры  и
и  определяют экспериментально.
определяют экспериментально.
Короткодействие сил отталкивания используют в идеализированной модели для газов: молекулы и атомы рассматриваются, как упругие шарики, при столкновении которых возникают большие силы отталкивания.
|
Дата добавления: 2014-01-06; Просмотров: 330; Нарушение авторских прав?; Мы поможем в написании вашей работы!