
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Принципы и основные характеристики плазмохимического травления
|
|
|
|
В ИПТ, рассмотренном в предыдущем параграфе, для травления используется ионно-плазменное распыление. Мишенью при этом служат обрабатываемые пластины. Однако такой метод травления малоэффективен, недостаточно селективен, требует больших энергий частиц, вследствие чего появляется опасность повреждения обрабатываемой структуры элементов МРЭУ.
Селективность травления является одним из важнейших факторов при формировании конфигураций элементов МРЭУ, так как травление не должно идти глубже требуемого слоя и затрагивать близлежащие слои. Чтобы повысить эффективность ИПТ, можно использовать энергию разряда для синтеза химически активных частиц (ХАЧ) в плазме, которые быстро и селективно травят данную поверхность. Такие процессы называются плазмохимическим травлением (ПХТ). Поскольку вещества при плазмохимических методах травятся с высокими избирательностью и скоростью, эти методы более эффективны для технологии МРЭУ, чем простое ИПТ. В зависимости от значений давления, энергии и наличия реагентов характер процесса травления может варьироваться от чисто физического до чисто химического.
Рассмотрим ПХТ твердой поверхности материалов, применяемых в технологии МРЭУ. Поскольку теоретические аспекты ПХТ наиболее полно изучены применительно к кремниевым пластинам, изложение термодинамики, механизма и кинетики рассматриваемых процессов целесообразно базировать на данных, полученных для кремниевых пластин.
В общем случае взаимодействие ионизированного газа с поверхностью твердого тела можно записать в виде следующей реакции:
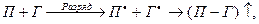 Разряд:
Разряд:
(454 11.8)
 где П, П*— нейтральный и активированный атомы на поверхности твердой подложки; Г, Г*— нейтральные и активированные в плазме атомные частицы газа-реагента; (П—Г) — летучее соединение веществ подложки и активного газа.
где П, П*— нейтральный и активированный атомы на поверхности твердой подложки; Г, Г*— нейтральные и активированные в плазме атомные частицы газа-реагента; (П—Г) — летучее соединение веществ подложки и активного газа.
|
|
|
Для кремния и фтора реакция (454) запишется следующим образом:
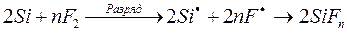
(455 11.9)
при n£4.
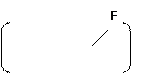
Реакция (455) протекает в несколько стадий. Сначала атомы фтора хемосорбируются на поверхности кремния с образованием прочной ковалентной связи, которая ослабляет связь атомов кремния с кристаллической решеткой. Атомы фтора индуцируют электроны атомов кремния. В результате индукционного эффекта смещаются электроны атомов кремния, расположенных в более глубоких приповерхностных слоях. Это приводит к ослаблению их связей с кристаллической решеткой. Атомы фтора легко превращают такие атомы в летучее соединение SiF4. Запишем схемы реакций этих стадий:
 | |||
 | |||

|








 Si Si F + F* Si Si (456 11.10)
Si Si F + F* Si Si (456 11.10)
 | |||
 | |||

|




|


 Si Si + F* Si Si F (457 11.11)
Si Si + F* Si Si F (457 11.11)
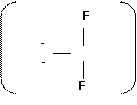 | |||
 | |||




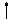
 Si Si F + F* Si + SiF4 (458 11.12)
Si Si F + F* Si + SiF4 (458 11.12)
 |
Согласно (456)—(458) образуются новые активные центры иа поверхности кремния, которые, в свою очередь, вступают в реакцию с атомами фтора по схеме (454):

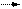 Si* + 4F* SiF4 (459 11.13)
Si* + 4F* SiF4 (459 11.13)
Следует подчеркнуть, что в плазме в результате бомбардировки сорбированных частиц ее компонентами (ионами, электронами) на поверхности могут отрываться не только молекулы SiF4, но и радикалы SiF, SiF2, SiF3. Такие активные газы, как F2, Cl2, Br2,неследует использовать при травлении, так как они разрушают практически все конструкционные материалы в промышленных установках. Поэтому на практике применяются неагрессивные рабочие среды, содержащие галогены (CF4, CCl4 и др.), которые под действием плазмы диссоциируют с образованием в зоне плазмы активных частиц F*, C1* и т. п. Под действием плазмы могут протекать н более сложные реакции (табл. 11.3). Здесь будут рассмотрены основные из них, связанные с возбуждением и диссоциацией.
|
|
|
Процессами, определяющими механизм и кинетику травления, являются диссоциация и активация галоген-содержащих газов. Рассмотрим их на примере диссоциации CF4. Реакции диссоциации молекул CF4 в низкотемпературной плазме имеют вид:
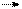 CF4 + е СF*3 + F* + е (460 11.14)
CF4 + е СF*3 + F* + е (460 11.14)
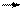 CF4 + е СР3+ + F* + 2 е (47011.15)
CF4 + е СР3+ + F* + 2 е (47011.15)
 СF4 + е СF*3 + F– (47111.16)
СF4 + е СF*3 + F– (47111.16)
Экспериментальные данные показывают, что преобладающей является реакция (460 11.14).
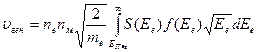 Для реализации эффективного ПХТ твердой поверхности необходимо осуществить диссоциацию рабочего газа, которая определяет скорость генерации uген ХАЧ в плазме разряда:
Для реализации эффективного ПХТ твердой поверхности необходимо осуществить диссоциацию рабочего газа, которая определяет скорость генерации uген ХАЧ в плазме разряда:
(472 11.17)
где nе, n м—концентрация электронов и молекул газа, из которых образуются энергетические и химически активные частицы; mе— масса электрона; Ее— энергия электронов; S(Eе)— сечение взаимодействия электронов и молекул; f(Eе) — функция распределения электронов по энергиям; Е п .е — пороговая энергия процесса образования энергетических и химически активных частиц.
Таблица 1Типы реакций, протекающих в плазме
| Вид плазменного воздействия | Тип реакции | Схема реакции |
| Электронный удар | Возбуждение Диссоциация Ионизация Диссоциативная ионизация | АВ+е АВ* + е АВ+е АВ* А+В+е АВ+е АВ+ +2 е АВ+е А++В+2е |
| Неупругие столкновения между тяжелыми частицами | Ионизация Ион-атомная рекомбинация Ион-ионная рекомбинация Электрон-ионная рекомбинация Атомная рекомбинация Атомный обмен Атомное дополнение | М + А2 А2+ + М + е А– + A А2 + е M– + А2+ А2 + М e + А2+ 2A 2A + M А2 + М А + ВС АВ + С А + ВС + М АВС + М |
| Гетерогенные реакции | Атомная рекомбинация Стабилизация частиц Распыление | [S п – A] + A S п + A2 S п + A* S п + A [S п – A] + M* S п + A + M |
   Излучение плазмы (hv) Излучение плазмы (hv)
| Диссоциация Ионизация Возбуждение | AB + hv A + B АВ + hv A+ + В– АВ + hv AB* |
Примечание. А, В, С— атомы вещества; М —молекула (радикал); е— электрон; A *, М*, АВ* — возбужденные атом, молекула и соединение АВ;A+, B+, М+ и A–, В–, М– — положительные и отрицательные ионы; Sп—площаь поверхности твердого тела; hv —квант излучения.
Из (472 11.17) следует, что скорость uген можно аналитически рассчитать при известных функции распределения электронов f(Eе) и сечении взаимодействия S(Eе). Вид функции распределения находится из кинетического уравнения Больцмана на основании законов взаимодействия частиц. К сожалению, пока нет аналитических выражений для всех функций возбуждения и ионизации. Поэтому уравнение (472 11.17) можно решить только для некоторых типов разрядов в одноатомных и двухатомных газах. В остальных случаях используют приближенные выражения.
|
|
|
Рассмотрим два основных вида распределения электронов. Первый—распределение по энергиям (распределение Дрюйвестейна), возникающее вследствие потери энергии электронов за счет упругих столкновений при длине пробега lе, не зависящей от энергии:


 f д (Eе)= 1,04(Eе)-3/2exp(-0,55(Eе/ Eе)2) Eе 1/2, (473 11.18)
f д (Eе)= 1,04(Eе)-3/2exp(-0,55(Eе/ Eе)2) Eе 1/2, (473 11.18)
 где E е = 0,5 mе u e 2 — средняя энергия электронов.
где E е = 0,5 mе u e 2 — средняя энергия электронов.
Второй случай — распределение Максвелла, учитывающее взаимодействие между электронами, а именно их взаимное отталкивание, приводящее к изменению энергии:
 f м (Eе) =(27/2p)1/2(Eе)-3/2exp(-1,5 Eе/ Eе) Eе 1/2, (474 11.19)
f м (Eе) =(27/2p)1/2(Eе)-3/2exp(-1,5 Eе/ Eе) Eе 1/2, (474 11.19)
Для максвелловского распределения вводится понятие электронной температуры Te = 2Ee/(3k). Тогда выражение (474 11.19) можно переписать в виде
f м (Eе) =(2/p1/2) (kTе)-3/2exp(-0,5 Eе/ kTе) Eе 1/2. (475 11.20)
При равной средней энергии электронов для максвелловского распределения в плазме содержится значительно больше быстрых электронов, чем для распределения Дрюйвестейна. Перенос электронов (диффузия и дрейф) зависит от средней энергии, а ионизация и возбуждение атомов—от числа электронов с высокой энергией на “хвосте” распределения.
Максвелловское распределение наиболее точно характеризует распределение электронов в плазме молекулярных газов, поскольку в этих газах уровни возбуждения изменяются от потенциала основного состояния до потенциала ионизации. Потери энергии для неупругих столкновений происходят при относительно низких ее значениях. В инертных газах уровни возбуждения ближе к потенциалу ионизации. Таким образом, при малых Е/р важны только потери, обусловленные упругими столкновениями. Средняя энергия электронов Ее в инертных газах намного выше, чем в молекулярных газах при одинаковом значении Е/р. В этом случае можно применить распределение Дрюйвестейна.
|
|
|
Энергия Ее является характеристикой функции распределения электронов по энергиям, она определяется отношением Е/р. Значение Е/р контролировать значительно проще, чем находить Ее. Следовательно, отношение Е/р — важный параметр, позволяющий оценить скорость генерации энергетических и химически активных частиц в газоразрядной плазме. Другими параметрами, необходимыми для вычисления скорости генерации энергетических и химически активных частиц, являются сечения ионизации и диссоциации.
Подставив в (472 11.17) функцию распределения Максвелла из (475 11.20) и сечение диссоциации молекул CF4 из табл. 11.4, получим выражение для скорости генерации ХАЧ CF*3 и F*:
uген= n e n мexp(–1,45*103/ Te)(7,74*10-17 Te 1/2 + 1,03*10-2 Te 3/2). (476 11.21)
Одновременно с реакциями диссоциации CF4 в плазме происходят рекомбинация радикалов СР*3 и атомов F, среди которых можно выделить гетерогенные:
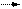 CF*3 + F* + Sп CF*3 + Sп(477 11.22)
CF*3 + F* + Sп CF*3 + Sп(477 11.22)
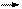 F* + F* + Sп F*2 + Sп (478 11.23)
F* + F* + Sп F*2 + Sп (478 11.23)



 CF*3 + CF*3 + Sп C2F*6 + Sп (479 11.24)
CF*3 + CF*3 + Sп C2F*6 + Sп (479 11.24)
и гомогенные:
CF*3 + F* + M CF*4 + M (480 11.25)
F* + F* + M F*2 + M (481 11.26)
CF*3 + CF*3 + M C2F*6 + M (482 11.27)
где M — частица (обычно молекула CF4).
В плазме CF4 без добавок кислорода количество образующегося С2F6 очень мало, поэтому реакциями (479 11.24) и (482 11.27) можно пренебречь. Реакциями (478 11.23) и (481 11.26) также можно пренебречь по сравнению с реакциями
(477 11.22) и (480 11.25), так как время жизни возбужденной молекулы F3* до стабилизации ее при ударе третьей частицей на 3–5 порядков меньше времени жизни возбужденной молекулы CF4*. Вероятность реакции (477 11.22) возрастает с понижением, а реакции (480 11.25) —с повышением давления. Реакция (480 11.25) протекает в три стадии:
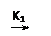 |
CF3* + F* CF4*
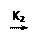 |
CF4* + M CF4 + M
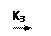 |
CF4* CF3* + F*
где K1, K2, K3—константы скоростей химических реакций.
На первой стадии из-за перераспределения энергии взаимодействия по связям образуется короткоживущая частица CF4*. На второй стадии избыточное количество энергии передается третьей частице М с образованием стабильной молекулы CF4. На третьей стадии происходит распад CF4* в случае, когда она не сталкивается с третьей частицей. Скорость реакции образования стабильных молекул CF4 описывается уравнением
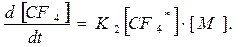
(483 11.29)
В течение некоторого времени концентрация промежуточного продукта CF4* остается постоянной, поэтому
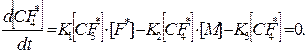 (484 11.30)
(484 11.30)
Отсюда
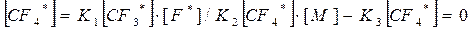
(485 11.31)
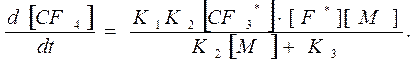 Подставив выражение (485 11.31) в (483 11.29), найдем
Подставив выражение (485 11.31) в (483 11.29), найдем
(486 11.32)
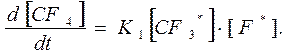 Величина 1/ К3 представляет собой среднюю продолжительность жизни нестабильной частицы CF4*, которая велика по сравнению со временем 1/K2 между ее соударениями с частицалщ М. Поэтому значением К3 в знаменателе (486 11.32) можно пренебречь. Тогда
Величина 1/ К3 представляет собой среднюю продолжительность жизни нестабильной частицы CF4*, которая велика по сравнению со временем 1/K2 между ее соударениями с частицалщ М. Поэтому значением К3 в знаменателе (486 11.32) можно пренебречь. Тогда
(487 11.33)
Таким образом, реакция (480 11.25) хотя и протекает при одновременном взаимодействии трех частиц, но описывается биомолекулярным законом. Скорость гомогенной рекомбинации свободных атомов F и радикалов СF3*
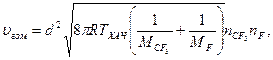
(488 11.34)
где d =0,5(d CF3 + d F); d CF3, d F —диаметры радикалов СF*3 и атомов F; R=8,314 Дж/(моль*К) —универсальная газовая постоянная; TХАЧ—температура атомов F и радикалов СF*3, которая в первом приближении равна температуре молекул CF4; MCF3, MF и n CF3, n f— относительные молекулярные массы и равновесные концентрации радикалов СF3 и атомов F.
Поскольку d F=1,4*10-10м, d CF3=2,8*10-10м, d =2,12*10-10м, в выраженнии (488 11.34) неизвестными останутся только концентрации n F и n CF3, радикалов F* и СF3*. Если начальная концентрация молекул газа CF4 в плазмохимическом реакторе n м, а концентрация молекул газа CF4 в плазме разряда n мп, то
n хач = nF = nCF3 = n м – n мп . (489 11.35)
где n хач —концентрация ХАЧ в плазме.
Подставив выражение (489 11.35) в (488 11.34) и проведя вычисления, получим следующее выражение для скорости гомогенной рекомбинации радикалов СF3* и атомов F в плазме разряда:
uгом =1,69•10-19 (TХАЧ) 1/2 (n м – n мп)2 . (490 11.36)
Процессы диссоциации молекул CF4 и рекомбинации атомов F с радикалами СF*3 в плазме разряда со временем приходят в равновесие, поэтому можно приравнять выражение (476 11.21) и (490 11.36) и после преобразования получить уравнение
n 2мп – 2 n м(n мп + B) + n2 м=0, (491 11.37)
где
B = n e/(Tхач)1/2(220Te1/2 + 3,05•10-3Te3/2)exp(–1,45•105/Te). (492 11.38)
Решив уравнение (491 11.37) с учетом (489 11.35), найдем
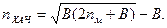
(492 11.39)
Определив температуру и концентрацию электронов в плазме разряда, а также температуру газа в реакторе, можно по формулам (492 11.38) и (492 11.39) вычислить стационарные концентрации молекул CF4, атомов F и радикалов СF3* в плазме разряда. Полученные значения хорошо согласуются с экспериментальными результатами.
Приведенная методика расчета стационарной концентрации ХАЧ в плазменной зоне реактора отвечает условию, при котором скорость гибели ХАЧ определяется гомогенной объемной рекомбинацией. Однако причиной гибели ХАЧ может являться и их гетерогенная рекомбинация на стенках реактора. Этот процесс состоит из двух стадий: диффузии ХАЧ к стенкам реактора и захвата ХАЧ стенками. Наиболее медленная из этих стадий определяет скорость гетерогенной рекомбинации. Если лимитирующей стадией является диффузия, то гетерогенная рекомбинация называется диффузионной и ее скорость характеризуется скоростью диффузии ХАЧ к стенкам реактора, а если взаимодействие ХАЧ с твердой поверхностью, то гетерогенная рекомбинация называется кинетической.
Кинетическая гетерогенная рекомбинация реализуется, когда вероятность взаимодействия ХАЧ с поверхностью при их соударении меньше 10-3. В этом случае происходит более тысячи соударений атома или радикала с поверхностью, прежде чем наступает их гибель. Поэтому можно с достаточной степенью точности считать, что концентрация ХАЧ в плазменной зоне реактора стационарна и не зависит от времени. Число ХАЧ, ударяющихся о стенку реактора площадью Sп в единицу времени,
N p= n ХАЧ [ k TХАЧ/(2p m ХАЧ)]1/2 Sп , (493 11.40)
где k— постоянная Больцмана; m хач —масса ХАЧ.
Скорость uгет гибели ХАЧ в единице объема плазменной зоны реактора определяется произведением числа ХАЧ, ударяющихся о его стенку, на вероятность Р их взаимодействия со стенкой, деленному на объем Vп.з плазменной зоны:
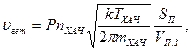
(493 11.41)
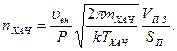 В стационарном состоянии скорость генерации ХАЧ в единице объема плазменной зоны равна скорости их гибели за счет гетерогенной рекомбинации, поэтому
В стационарном состоянии скорость генерации ХАЧ в единице объема плазменной зоны равна скорости их гибели за счет гетерогенной рекомбинации, поэтому
(494 11.42)
Подставив в выражение (494 11.42) значение uген из (476 11.21), можно найти стационарную концентрацию ХАЧ, которая будет обратно пропорциональна вероятности взаимодействия ХАЧ с материалом стенок реактора и площади поверхности.
При диффузионой гетерогенной рекомбинации скорость гибели ХАЧ на стенках реактора велика, и вероятность взаимодействия Р близка к единице. В этом случае стационарная концентрация ХАЧ в плазменной зоне определяется из решения уравнения непрерывности.
Отношение стационарной концентрации ХАЧ в плазменной зоне к исходной концентрации молекул рабочего газа характеризует степень плазмохимической диссоциации:
aдис= n ХАЧ+ n м.
 Степень плазмохимической диссоциации или степень превращения молекул рабочего газа в ХАЧ в плазменной зоне реактора зависит от времени tпл нахождения молекул газа в плазменной зоне, энергии Ее и концентрации nе электронов в плазме, вида и состава рабочего газа, материала стенок реактора. Она может иметь значение от долей до десятков процентов.
Степень плазмохимической диссоциации или степень превращения молекул рабочего газа в ХАЧ в плазменной зоне реактора зависит от времени tпл нахождения молекул газа в плазменной зоне, энергии Ее и концентрации nе электронов в плазме, вида и состава рабочего газа, материала стенок реактора. Она может иметь значение от долей до десятков процентов.
|
|
|
|
Дата добавления: 2014-01-07; Просмотров: 503; Нарушение авторских прав?; Мы поможем в написании вашей работы!